前言
烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide,NAD+) 是细胞内一种重要的辅助调节因子,参与细胞能量代谢、蛋白翻译后修饰、DNA修复和细胞应激适应等生物过程,NAD+代谢紊乱与多种生理改变、病理损伤及疾病的发生发展密切相关,涉及生物衰老进程、代谢性和神经退行性疾病以及各种癌症。通过调节NAD+代谢,恢复细胞内NAD+水平,显示了对细胞功能和相关疾病的有益效果。本文综述了NAD+的代谢以及在细胞功能、相关疾病进程的调控作用,并讨论了这一研究领域可能存在的治疗意义。
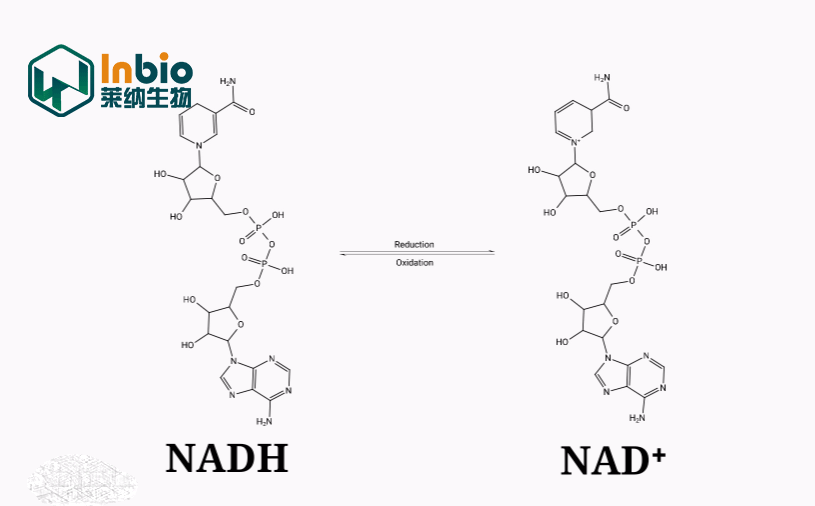
NAD+,即辅酶Ⅰ,在细胞内主要有两种形式: 即氧化型( NAD+) 和还原型(NADH) ,两者是氧化或还原反应中介导氢转移的一对酶辅助因子,NAD+/NADH比例的稳态在氧化还原反应中对于维持生物能的产生至关重要。除此以外,近年来研究发现,NAD+除了参与氧化还原功能外,还调控了细胞内许多重要信号传导过程,例如: 作为细菌DNA连接酶、ADP核糖基转移酶或聚核糖基聚合酶(poly ADP-ribose polymerases,PARPs) 、环ADP核糖合成酶( cyclic ADP-ribose synthases,cADP合酶) 和Sir2样蛋白去乙酰化酶( sirtuins,SIRT) 等信号传导酶的辅助催化底物,进而影响信号传导酶的催化活性及调节功能。NAD+将细胞代谢与生理信号传导直接联系起来,在调节细胞的生长节律、分化衰老、应激适应和疾病发生等生命过程中起到关键作用,针对NAD+代谢及其调节机制的研究可能是疾病治疗的一个有希望靶点。
2.1 NAD+的消耗
NAD+是NAD+依赖型ADP核糖基转移酶的共同底物,这类酶在体内主要有3种,分别为PARP、cADP合酶和Sirtuins。这类酶会将 NAD+分解成ADP核糖和烟酰胺( nicotinamide,NAM) ,在不同细胞中发挥不同生理功能。然而,这一过程同样也导致了NAD+被消耗。其中,PARP是细胞中NAD+的主要消耗者,在DNA修复过程中起着重要作用。通过将NAD+作为底物转移ADP核糖基到 DNA修复相关蛋白,使其活化,参与DNA修复、基因组稳定、染色质重建等基因修复过程。cADP合酶消耗NAD+是通过产生环状 ADP-核糖 ( cADP-ribose,cADPR) 。cADPR是钙和胰岛素信号中强有力的第二信使,在免疫应答和维持钙离子稳态方面具有重要意义。Sirtuins是一个由7种蛋白( Sirt1-7) 组成的家族,它们具有去乙酰化酶、去丙二酰化酶、脱琥珀酰化酶和去戊二酰化酶活性,其中 sirtuins的脱乙酰基或脱酰基需要NAD+作为共底物,将乙酰化蛋白质中的赖氨酸转移至NAD+中的ADP核糖基,形成一个新的去乙酰化蛋白质和NAM。以上3种酶承担了NAD+的主要消耗过程,在细胞不同的亚结构中、不同的病理生理过程中,每种消耗酶占主导地位不尽相同,但是,NAD+的产生和消耗之间的最佳平衡对于调节各种病理生理条件下多种生物过程至关重要。
2.2 NAD+的生物合成
NAD+在发挥其生物学功能过程中会被消耗,需要不断合成以维持细胞内NAD+稳态。NAD+的生物合成主要有两条途径:从头合成途径和补救合成途径。从头合成途径中,由色氨酸衍生的喹啉酸(quinolinic acid,QA) 是从头合成途径的主要起始成分。生成的QA被用来产生中间产物烟酸单核苷酸(nicotinic acid mononucleotide,NAMN) ,NAMN通过烟酰胺单核苷酸腺苷转移酶(nicotinamide mono- nucleotide adenylyl transferases,NMNATs) 催化作用生成烟酸腺嘌呤二核苷酸(nicotinic acid adeninedi- nucleotide,NAAD) ,NAAD又在NAD合成酶的催化下,最终生成NAD+。但是,通过此途径合成的NAD+仍不足以维持机体正常的NAD+需要,细胞还需要经由补救合成途径来产生 NAD+。
在补救合成途径中,NAD+从前体烟酰胺核苷(nicotinamide riboside,NR) 、烟酸(nicotinic acid,NA)或NAM中再生。NAM 可被烟酰胺磷酸核糖转移酶( nicotinamide phosphotransferase,NAMPT) 转化为烟酰胺单核苷酸(nicotinamide mononucleotide,NMN) ,NMN还可以由烟酰胺核糖核苷激酶(nico- tinamide riboside kinase,NRK) 对NR进行磷酸化生成,最终NAMN和NMN都是被NMNATs腺苷化为NAD+。在细胞中,通过前体补救途径合成在维持细胞NAD+生理水平中最为重要。
3、NAD+下降导致细胞功能障碍
NAD+是糖酵解和氧化磷酸化过程中线粒体最大氧化能力的限制因素,NAD+稳态受损将会影响细胞代谢功能及氧化还原平衡,这主要和线粒体功能障碍有关。细胞在糖酵解和三羧酸循环过程中产生NADH而导致还原性应激,需要通过线粒体将NADH再氧化生成NAD+来维持细胞中NAD+/NADH比值稳定,这对于葡萄糖的持续氧化、ATP的产生和正常细胞功能必不可少。线粒体功能障碍导致氧化呼吸链缺陷和糖酵解增加,产生过量NADH,不能被氧化为NAD+,破坏NAD+/NADH稳态,导致细胞产生还原应激状态。而低水平的NAD+影响线粒体ATP合成并又会增加活性氧(reactive oxygen species,ROS)产生,过量产生的ROS引起线粒体DNA(mitochondrial DNA,mtDNA) 突变,可导致呼吸链缺陷和刺激糖酵解。呼吸链缺陷则又会产生更多的ROS,加重对线粒体的损伤,最终形成恶性循环。线粒体功能持续恶化将影响细胞内的代谢和氧化还原平衡,导致细胞功能障碍,甚至凋亡。因此,调控细胞内 NAD+水平稳态对细胞功能的保护作用可能是通过改善线粒体功能来实现。
4、NAD+与疾病
越来越多研究表明代谢和年龄相关疾病与NAD+稳态受损密切相关。例如:衰老、年龄相关的听力障碍、心脏缺血/再灌注损伤和心肌病,都会出现NAD+水平下降。因此,恢复NAD+水平可能是治疗这些疾病的一种有希望的方法。
4.1 补充NAD+延缓衰老
NAD+代谢与衰老关系密切。在大鼠衰老模型中发现NAD+/NADH比值随着年龄的增长而显著下降,并且NAD+代谢紊乱会引起多种与衰老相关疾病的发生。相反,NAD+水平的上调,包括膳食中添加NAD+前体,已被证明可以预防NAD+的下降,并显示出对衰老和衰老相关疾病的有益作用。在秀丽隐杆线虫和果蝇早衰疾病模型中通过NAD+补充显著延长了其寿命并延缓衰老表型。为什么NAD+水平会随着年龄的增长而下降?一种可能性是一个或多个NAD+生物合成途径异常。如上所述,NAMPT是NAD+补救合成途径的关键酶,NAMPT受昼夜节律转录因子BMAL和CLOCK的调控。当昼夜节律机制的活动随着年龄的增长而系统性下降,则会导致NAMPT和NAD+的缺乏。在这种情况下,使用NMN或NR等NAD+前体,将是有效促进NAD+生物合成,延缓衰老的关键。
4.2 NAD+缓解听力损伤
听力障碍是最常见的感觉障碍,在残疾人群中占有很大的比例,针对其病因所采取的治疗方法有很多,但目前关于其分子治疗的研究仍十分有限。通过对NAD+水平的直接调节对听力障碍有缓解作用。针对噪声引起支配耳蜗毛细胞的螺旋神经节变性而导致听力损失的研究中,通过给小鼠注射NR来提高小鼠耳蜗NAD+水平,激活了NAD+ -Sirt3通路,减少了噪声暴露引起的轴突变性,能防止噪声性听力损失(NIHL)。此外,对于年龄相关性听力损失研究表明衰老过程中毛细胞 NAD+的减少是年龄相关性听力损失(ARHL) 的重要原因,通过恢复NAD+水平可改变多种信号传导途径,减少耳蜗组织的氧化应激和炎性反应,例如NF-κB、p53、Sirt3和IDH2。同时,NAD+调节还可以通过促进恢复毛细胞数量和受损带状突触形成,从而改善耳蜗对听觉刺激应答过程中的突触传递,以挽救听力丧失。耳毒性是接受顺铂化疗的患者的一个重要不良反应,最近的研究表明,细胞内NAD+水平的紊乱与顺铂诱导的耳蜗氧化应激、DNA损伤和炎性反应有着密切联系,细胞内NAD+/NADH比率降低在顺铂诱导的耳蜗损伤中可能起着关键作用,提高细胞内NAD+/NADH比率,可以降低潜在的细胞损伤介质,如氧化应激和炎性反应来抑制顺铂诱导的耳蜗损伤。NAD+对过量锰造成的听觉系统的耳毒性和神经毒性同样具有保护作用,NAD+可以预防锰引起的轴突变性,避免锰暴露引起的听力损失。因此,通过这些研究,发现NAD+可能是与听力障碍密切相关的生物调节因子,对其分子机制的进一步研究,有望开辟新的分子治疗靶点。
4.3 NAD+的心脏保护作用
心脏损伤也会引起NAD+水平的变化。NAD+失调参与了许多心血管疾病过程。因此,补充NAD+的前体可能具有心脏保护作用。心肌缺血再灌注(IR)损伤下用NMN预处理小鼠可以有效地防止与缺血相关的NAD+下降,并对心脏IR有保护作用。心肌肥厚也与NAD+稳态的改变有关。在血管紧张素II诱导的心肌肥厚的小鼠模型中,细胞内NAD+水平明显降低,通过NAD+给药激活Sirt3,可阻断血管紧张素II诱导的心肌肥厚。线粒体电子传递链功能受损会导致NAD+/NADH比值下降,增加线粒体蛋白乙酰化水平,容易发生心肌肥大和衰竭,而在晚期心力衰竭动物模型和人类患者的心脏组织中也发现NAD+氧化还原失衡和蛋白乙酰化增加。重要的是,NMN可使这些衰竭心脏的NAD+氧化还原失衡恢复正常,抑制病理性心肌肥大,改善心功能。最近在遗传性或扩张性心肌病小鼠模型中也证明了NMN在恢复心功能和改善心脏功能方面的功效,提高NAD+水平对治疗心肌病具有有益作用。基于上述研究基础,以NAD+作为治疗靶点,通过补充恢复心肌内NAD+水平来干预治疗,对心肌的保护具有广泛影响,对多种心脏疾病也可以产生治疗和预防作用。
NAD+是细胞内重要的辅助因子,其作用不仅仅局限在对氧化还原反应的调节,更多的是表现为其非氧化还原反应的调节作用。其广阔的生理作用仍需要进一步研究,NAD+的代谢对人类健康维持和疾病的发生影响重大,回顾研究清楚地表明,NAD+水平在衰老、听力损伤、心脏疾病等许多疾病过程中下降,与疾病的发生关系密切。NAD+代谢及相关调节途径提示,NAD+的补充可能有益于疾病的转归和恢复。通过以NAD+为治疗靶点,干预NAD+的代谢和调节相关代谢途径靶酶可能是许多年龄相关性、代谢性和神经退行性疾病、各种癌以及生物衰老的一种潜在的、有效的治疗方法。